Il tuo carrello è vuoto!
Categorie
- Acque Minerali
+-
- Alimentazione E Dietetica
+-
- Antimicrobici Generali Per Uso Sistemico
+-
- Apparato Gastrointestinale E Metabolismo
+-
- Articoli Sanitari E Dispositivi Medici
+-
- Apparecchiature
- Articoli Sanitari Per Casa E Ambiente
- Biocidi/Presidi Medico-Chirurgici
- Casa E Ambiente
- Contraccezione E Profilassi
- Diagnostici
- Dispositivi Per Somministrazione Di Sostanze Terapeutiche
- Dpi Dispositivo Di Protezione Individuale
- Medicazione (Strumenti E Materiale Per)
- Occhiali/Lenti E Accessori
- Ortopedia E Comfort Per La Persona
- Prodotti Antifumo
- Prodotti Per La Protezione Degli Apparati
- Puericultura Ed Infanzia
- Strumenti E Accessori Igienico-Sanitari
- Strumenti per Autodifesa Non Idonei ad Arrecare Offesa
- Strumenti Sanitari (Altri)
- Dermatologici
+-
- Descrizione Alternativa
- Erboristeria E Fitoterapia
+-
- Farmaci Antiparassitari, Insetticidi E Repellenti
+-
- Galenica
+-
- Igiene E Cosmesi
+-
- Omeopatia E Medicina Naturale
+-
- Organi Di Senso
+-
- Preparati Ormonali Sistemici,Escl.Ormoni Sessuali E Insuline
+-
- Sangue Ed Organi Emopoietici
+-
- Sistema Muscolo-Scheletrico
+-
- Sistema Nervoso
+-
- Sistema Respiratorio
+-
- Vari
+-
- Veterinaria
+-
- Alimentazione E Dietetica Veterinaria
- Animali (Accessori Per)
- Animali (Altri Prodotti Per)
- Antiparassitari Veterinari
- Diagnostici Uso Veterinario
- Disinfettanti E Prodotti Per L'Ambiente Uso Veterinario
- Medicazione Uso Veterinario (Strumenti E Materiale Per)
- Medicinali Veterinari
- Omeopatici Veterinari
- Toelettatura
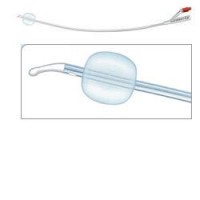
LIQUICK PLUS CATET ERGO CH14
LIQUICK PLUS CATETERE
Dispositivo medico CE di classe Is; per cateterismo vescicale intermittente.Caratteristiche
Kit costituito da catetere vescicale in punta ergothan / olivare ad una via, autolubrificante, con sacca graduata integrata da 800 ml. Viene fornito anche un blister di soluzione fisiologica e un telino d’appoggio.
Gamma Prodotto
| Codice Prodotto | Ch | Punta | Lungh. Cm | Numero fori | Numero vie |
| 620012 CH 12 | 12 | Ergothan / Olivare | 40 | 2 | 1 – con sacca urina integrata |
| 620014 CH 14 | 14 | Ergothan / Olivare | 40 | 2 | 1 – con sacca urina integrata |
| 620016 CH 16 | 16 | Ergothan / Olivare | 40 | 2 | 1 – con sacca urina integrata |
| 620210 CH 10 | 10 | Ergothan / Olivare | 30 | 2 | 1 – con sacca urina integrata |
| 622012 CH 12 | 12 | Nelaton | 40 | 2 | 1 – con sacca urina integrata |
| 622014 CH 14 | 14 | Nelaton | 40 | 2 | 1 – con sacca urina integrata |
Presenza di lattice, ftalati (DEHP), farmaci, sostanze, tessuti biologici
| Descrizione | Si | No |
| Lattice | X | |
| DEHP | X | |
| Farmaci | X | |
| Sostanze | X | |
| Tessuti Biologici | X |
Contiene un blister di fisiologica.
Materiale di costruzione:
PVC ERU – RÜSCHELIT.
Descrizione materiale:
Eru – Rüschelit è il marchio registrato per il PVC usato da TELEFLEX MEDICAL nel settore medicale. A seconda della destinazione d’uso il materiale può essere più rigido o più morbido, trasparente o opaco. Queste proprietà conferiscono agli strumenti in RÜSCHELIT rigidità, stabilità e resistenza all’inginocchiamento. Durante il processo produttivo possono essere aggiunte particolari sostanze al fine di rendere il dispositivo radiopaco. RÜSCHELIT viene utilizzato principalmente per la realizzazione di strumenti flessibili all’interno dei quali può essere incorporata una spirale di acciaio inox. Al contatto con il calore corporeo, il materiale diventa più morbido, adattandosi in modo ottimale alle conformazioni anatomiche. Il lubrificante impiegato è un gel a base d’acqua, idrosolubile ed anallergico. La presenza di un introduttore e di una guida di scorrimento facilita il cateterismo ad intermittenza riducendo i rischi di contaminazioni batteriche. I fori del catetere sono smussati attraverso una metodica a taglio verticale. La punta olivare / Ergothan consente un inserimento graduale ed atraumatico. I materiali in Eru – Rüschelit sono controllati secondo le norme USPXXIII, classe VI e IS O10993, EN 30993.
Specifiche di sterilizzazione
Durata sterilizzazione: 1 anno dalla data di fabbricazione.
I prodotti Medical Service GmbH sono sterilizzati ad ossido di etilene come da normative EN 550:1994, EN ISO 10993- 7:1995. Le iscrizioni indicanti la data di sterilizzazione, la relativa scadenza e il numero di lotto appaiono chiaramente sulla confezione del prodotto. La sterilità non è garantita se la confezione non è integra. Utilizzare immediatamente dopo l’apertura della confezione. Prodotto monouso non risterilizzabile.
Incompatibilita chimico-fisiche dei materiali
Incompatibilita chimico-fisiche dei materiali verso sostanze con le quali potenzialmente possono venire a contatto:
- Grassi e oli, come vasellina ed olio di paraffina;
- Solventi organici come benzolo ed etere;
- Materiali ossidanti come acqua ossigenata, zolfo ipoclorite;
- Disinfettanti contenenti fenolo o similari.
Modalità di confezionamento
La confezione del prodotto è stata studiata per consentire una buona conservazione della stessa e il facile immagazzinamento per sovrapposizione. Ogni confezione riporta in modo chiaro e ben leggibile, in lingua italiana, la descrizione qualitativa e quantitativa del contenuto, il nome del produttore e ogni altra informazione utile all'immediato riconoscimento del prodotto stesso. Le singole confezioni sono di facile apertura, tali da non permettere che il materiale aderisca alla confezione, facilitando il prelievo del prodotto.
Materiale utilizzato per la confezione primaria
Il prodotto viene confezionato mediante un imballo realizzato da uno strato di polietilene a bassa densità e da una pellicola di carta laccata rinforzata, garantendo inoltre un’ottima resistenza all’urto o alla trazione.
Quantità per confezione secondaria: uso domiciliare / territoriale
Una confezione secondaria contiene 30 pezzi, imbustati singolarmente.
Modalità di conservazione
Conservare a temperatura ambiente, lontano dall’esposizione diretta alla luce. Un’esposizione prolungata a luce fluorescente, luce del sole o calore danneggiano il dispositivo.
Modalità di smaltimento
Verificare le indicazioni dettate dalle normative Italiane inerenti lo smaltimento dei dispositivi medici.
Controlli di Qualità
I dispositivi sono progettati e fabbricati in modo che la loro utilizzazione non comprometta lo stato clinico e la sicurezza dei pazienti, né la sicurezza e la salute degli utilizzatori ed eventualmente di terzi, quando siano utilizzati alle condizioni e per i fini previsti.
Il CONTROLLO QUALITÀ, realizzato secondo le Normative Internazionali, prevede una serie di verifiche ad ogni stadio della produzione. Ogni lotto di produzione subisce un costante controllo tecnico-chimico-biologico dal momento dell'utilizzo della materia prima sino alla sterilizzazione. L’azienda certificata opera secondo un Sistema di Qualità in accordo alle G.M.P., EN ISO 14001, ISO 13485, EN 550 e secondo le M.D.D. 93/42.
Modalità di impiego e controindicazioni
Pregasi fare riferimento alle istruzioni per l’uso del prodotto.
Contenuto della confezione
Kit con: catetere, sacca, blister di soluzione fisiologica, telino.
Codice ISO: 092406015.
Certificato CE: 50955-17-01
Dichiarazione di conformità: Liquick® Plus_20.10.2010.
Nr. Repertorio: n / n.
CND: U01010501.
GMDN: 45603.
Cod. 620210CH10/ 620012CH12/ 620014CH14/ 620016CH16/ 622012CH12/ 622014CH14
Scrivi una recensione
Il Tuo Nome:La Tua Recensione: Nota: Il codice HTML non è tradotto!
Punteggio: Negativo Positivo
Inserisci il codice nel box seguente:
Altri prodotti di questo brand (6)